- Органы из пробирки: что уже умеют выращивать
- Интеллектуальные развлечения. Интересные иллюзии, логические игры и загадки.
- Добро пожаловать В МИР ЗАГАДОК, ОПТИЧЕСКИХ ИЛЛЮЗИЙ И ИНТЕЛЛЕКТУАЛЬНЫХ РАЗВЛЕЧЕНИЙСтоит ли доверять всему, что вы видите? Можно ли увидеть то, что никто не видел? Правда ли, что неподвижные предметы могут двигаться? Почему взрослые и дети видят один и тот же предмет по разному? На этом сайте вы найдете ответы на эти и многие другие вопросы.
- Log-in.ru© — мир необычных и интеллектуальных развлечений. Интересные оптические иллюзии, обманы зрения, логические флеш-игры.
- Интересно
- Выращивание органов из стволовых клеток
- Что такое стволовые клетки?
- Какие органы и ткани ученые смогли вырастить с помощью стволовых клеток?
- В 2005 году американские ученые впервые вырастили полноценные клетки головного мозга
- В 2005 году ученым удалось воспроизвести нервную стволовую клетку
- В 2006 году швейцарсцкие ученые вырастили из стволовых клеток клапаны человеческого сердца
- В 2006 году британские ученые вырастили из стволовых клеток ткани печени
- В 2006 году в США впервые выращен сложный человеческий орган — мочевой пузырь
- Американские ученые смогли вырастить в лабораторных условиях полноценный мочевой пузырь. В качестве материала были использованы клетки самих пациентов, нуждающихся в пересадке.
- В 2007 году стволовые клетки помогли британским ученым создать часть сердца человека
- В 2007 году японские ученые вырастили из стволовых клеток роговицу глаза
- В 2007 году японские ученые вырастили зуб из стволовых клеток
- В 2008 году американские ученые смогли вырастить новое сердце на каркасе от старого
- Искусственные органы: человек умеет все
- Запускаем печать
- Мозг под замену
- Нервный чип
- В новом теле
- Выращивание тканей и органов: мифы и реальность (лекция)
- В России обещают начать применять искусственные органы в трансплантологии
- Стволовые клетки и выращивание тканей и органов
Органы из пробирки: что уже умеют выращивать
Возможность вырастить человеческий орган в пробирке и пересадить его человеку, нуждающемуся в пересадке — мечта трансплантологов. Ученые по всему миру работают над этим и уже научились делать ткани, небольшие работающие копии органов, и до полноценных запасных глаз, легких и почек нам на самом деле осталось совсем немного. Пока что органеллы используются в основном в научных целях, их выращивают, чтобы понять, как работают органы, как развиваются болезни. Но от этого до трансплантации всего несколько шагов. МедНовости собрали сведения о самых перспективных проектах.
Легкие. Ученые из Техасского университета вырастили легкие человека в биореакторе. Правда, без кровеносных сосудов такие легкие не функциональны. Однако команда ученых из Медицинского центра Колумбийского университета (Columbia University Medical Center, New York) недавно впервые в мире получили функциональное легкое с перфузируемой и здоровой сосудистой системой у грызунов ex vivo.
Ткани сердечной мышцы. Биоинженерам из университета Мичигана удалось вырастить в пробирке кусок мышечной ткани. Правда, полноценно сердце из такой ткани пока работать не сможет, она вдвое слабее оригинала. Тем не менее пока это самый сильный образец сердечной ткани.
Кости. Израильская биотехнологическая компания Bonus BioGroup использовалат трехмерные сканы для создания гелеобразного каркаса кости перед посевом стволовыми клетками, взятыми из жира. Кости, получившиеся в результате, они успешно пересадили грызунам. Уже планируются эксперименты по выращиванию человеческих костей по этой же технологии.
Ткани желудка. Ученым под руководством Джеймса Уэллса из Детского медицинского клинического центра в Цинциннати (Огайо) удалось вырастить «в пробирке» трехмерные структуры человеческого желудка при помощи эмбриональных стволовых клеток и из плюрипотентных клеток взрослого человека, перепрограммированных в стволовые. Эти структуры оказались способны вырабатывать все необходимые человеку кислоты и пищеварительные ферменты.
Японские ученые вырастили глаз в чашке Петри. Искусственно выращенный глаз содержал основные слои сетчатки: пигментный эпителий, фоторецепторы, ганглионарные клетки и другие. Трансплантировать его целиком пока возможности нет, а вот пересадка тканей — весьма перспективное направление. В качестве исходного материала были использованы эмбриональные стволовые клетки.
Ученые из корпорации Genentech вырастили простату из одной клетки. Молекулярным биологам из Калифорнии удалось вырастить целый орган из единственной клетки.
Ученым удалось найти единственную мощную стволовую клетку в простатической ткани, которая способна вырасти в целый орган. Таких клеток оказалось чуть меньше 1% от общего числа. В исследовании 97 мышам трансплантировали такую клетку под почку и у 14 из них выросла полноценная простата, способная нормально функционировать. Точно такую же популяцию клеток биологи нашли и в простате человека, правда, в концентрации всего 0,2%.
Сердечные клапаны. Швейцарские ученые доктор Саймон Хоерстрап (Simon Hoerstrup) и Дорта Шмидт (Dorthe Schmidt) из университета Цюриха (University of Zurich) смогли вырастить человеческие сердечные клапаны, воспользовавшись стволовыми клетками, взятыми из околоплодной жидкости. Теперь медики смогут выращивать клапаны сердца специально для неродившегося еще ребенка, если у него еще в зародышевом состоянии обнаружатся дефекты сердца.
Ушная раковина. Используя стволовые клетки, ученые вырастили ухо человека на спине крысы. Эксперимент был проведен исследователями из Университета Токио (University of Tokyo) И Университета Киото (Kyoto University) под руководством Томаса Сервантеса (Thomas Cervantes).
Кожа. Ученые из Цюрихского университета (Швейцария) и университетской детской больницы этого города впервые сумели вырастить в лаборатории человеческую кожу, пронизанную кровеносными и лимфатическими сосудами. Полученный кожный лоскут способен почти полностью выполнять функцию здоровой кожи при ожогах, хирургических дефектах или кожных болезнях.
Поджелудочная железа. Ученые впервые создали васкуляризованные островки поджелудочной железы, способные вырабатывать инсулин. Еще одна попытка вылечить диабет I типа.
Почки. Ученые из австралийского университета Квинсленда научились выращивать искусственные почки из стволовых клеток кожи. Пока это лишь маленькие органоиды размером 1 см, но по устройству и функционированию они практически идентичны почкам взрослого человека.
Печень. Биологи сразу нескольких стран заявили о том, что смогли вырастить полноценный аналог печени, способный очищать кровь от токсинов и выполнять другие функции этого органа. Для этого ученые использовали стволовые клетки и «заготовки» из стволовых клеток. Эти разработки параллельно велись в Японии, Америке и России.
Мочевой пузырь. Группа американских ученых под руководством Энтони Аталы (Anthony Atala) вырастила в лаборатории человеческие мочевые пузыри, полностью готовые к пересадке, из образцов собственных тканей пациентов. Те же ученые вырастили мочеиспускательные каналы для пациентов, у которых они были повреждены.
Кроме того, ученые уже научились выращивать хрящевые ткани, ткани скелетных мышц и костей, ткани гипофиза, тимуса, а также ткани, функционирующие аналогично тканям человеческого мозга.
Интеллектуальные развлечения. Интересные иллюзии, логические игры и загадки.
Добро пожаловать В МИР ЗАГАДОК, ОПТИЧЕСКИХ
ИЛЛЮЗИЙ И ИНТЕЛЛЕКТУАЛЬНЫХ РАЗВЛЕЧЕНИЙСтоит ли доверять всему, что вы видите? Можно ли увидеть то, что никто не видел? Правда ли, что неподвижные предметы могут двигаться? Почему взрослые и дети видят один и тот же предмет по разному? На этом сайте вы найдете ответы на эти и многие другие вопросы.
Log-in.ru© — мир необычных и интеллектуальных развлечений. Интересные оптические иллюзии, обманы зрения, логические флеш-игры.
Привет! Хочешь стать одним из нас? Определись 

Если ты уже один из нас, то вход тут.
Интересно
«Венесуэла» по-испански означает «маленькая Венеция».
Выращивание органов из стволовых клеток
Прежде чем мы перейдем к непосредственному рассказу о выращивание органов, я хотел бы посвятить вас, что такое стволовые клетки.
Что такое стволовые клетки?
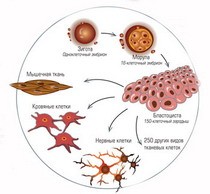
Стволовые клетки — прародительницы всех без исключения типов клеток в организме. Они способны к самообновлению и, что самое главное, в процессе деления образуют специализированные клетки различных тканей. Стволовые клетки обновляют и замещают клетки, утраченные в результате каких-либо повреждений во всех органах и тканях. Они призваны восстанавливать организм человека с момента его рождения.
С возрастом количество стволовых клеток в организме катастрофически снижается. У новорожденного 1 стволовая клетка встречается на 10 тысяч, к 20-25 годам – 1 на 100 тысяч, к 30 – 1 на 300 тысяч. К 50-летнему возрасту в организме уже остается всего 1 стволовая клетка на 500 тысяч. Истощение запаса стволовых клеток вследствие старения или тяжёлых заболеваний лишает организм возможностей самовосстановления. Из-за этого жизнедеятельность тех или иных органов становится менее эффективной.
Какие органы и ткани ученые смогли вырастить с помощью стволовых клеток?
Привожу только самые известные примеры научных достижений.
в 2004 году японские ученые впервые в мире вырастили структурно полноценные капиллярные кровеносные сосуды из стволовых клеток

Японские ученые первыми в мире вырастили структурно полноценные капиллярные кровеносные сосуды из стволовых клеток человеческого эмбриона. Об этом 26 марта 2004 года сообщила японская газета Yomiuri.
Как отмечает издание, группа исследователей из медицинской школы Киотского университета под руководством профессора Кадзува Накао использовала капиллярные клетки, генерированные из стволовых клеток, импортированных в 2002 году из Австралии. До сих пор исследователям удавалось регенерировать лишь нервные клетки и мышечную ткань, что недостаточно для «производства» цельного органа. Информация с сайта NewsRu.com
В 2005 году американские ученые впервые вырастили полноценные клетки головного мозга
Ученые из Флоридского университета (США) первыми в мире вырастили полностью сформированные и приживающиеся клетки головного мозга. Как сообщил руководитель проекта Бьорн Шеффлер, вырастить клетки удалось путем «копирования» процесса регенерации клеток головного мозга. Теперь ученые надеются выращивать клетки для трансплантации, что может помочь в лечении болезней Альцгеймера и Паркинсона.Шеффлер отметил, что ранее ученым удавалось выращивать нейроны из стволовых клеток, однако именно во Флоридском университете удалось получить полноценные клетки и изучить процесс их роста от начала до конца. Информация с сайта Газета.ру по материалам Independent.
В 2005 году ученым удалось воспроизвести нервную стволовую клетку
нервная стволовая клетка
Итальянско-британская группа ученых из эдинбургского и миланского университетов на основе неспециализированных эмбриональных стволовых нервных клеток научилась создавать in vitro различные типы клеток нервной системы.
Ученые применили уже разработанные методы управления эмбриональными стволовыми клетками к полученным ими более специализированным нервным стволовым клеткам. Результаты, которые были достигнуты на клетках мышей, были воспроизведены и на человеческих стволовых клетках. В интервью, данном агентству BBC, Стивен Поллард из Эдинбургского университета пояснил, что разработка его коллег поможет воссоздать болезнь Паркинсона или болезнь Альцгеймера «в пробирке». Это позволит лучше понять механизм их возникновения и развития, а также обеспечит фармакологов мини-полигоном для поиска подходящих средств лечения. Соответствующие переговоры с фармакологическими компаниями уже ведутся.
В 2006 году швейцарсцкие ученые вырастили из стволовых клеток клапаны человеческого сердца
Осенью 2006 года доктор Саймон Хоерстрап и его коллеги из университета Цюриха впервые вырастили человеческие сердечные клапаны, воспользовавшись стволовыми клетками, взятыми из околоплодной жидкости.
Это достижение может сделать реальным выращивание клапанов сердца специально для ещё не родившегося ребёнка, если у него, ещё в утробе матери, обнаружатся дефекты сердца. А вскоре после рождения младенцу можно будет пересадить новые клапаны.
Вслед за выращиванием в лаборатории из клеток человека мочевого пузыря и кровеносных сосудов — это следующий шаг на пути создания «собственных» органов для конкретного пациента, способных устранить потребность в донорских органах или искусственных механизмах.
В 2006 году британские ученые вырастили из стволовых клеток ткани печени
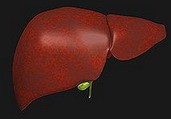
Осенью 2006 года британские ученые из университета Ньюкасла объявили о том, что первыми в мире вырастили в лабораторных условиях искусственную печень из стволовых клеток, взятых из пуповинной крови. Техника, которая использовалась при создании «минипечени», размером в 2 см, будет разрабатываться дальше, чтобы создать нормально функционирующую печень стандартного размера.
В 2006 году в США впервые выращен сложный человеческий орган — мочевой пузырь

Американские ученые смогли вырастить в лабораторных условиях полноценный мочевой пузырь. В качестве материала были использованы клетки самих пациентов, нуждающихся в пересадке.
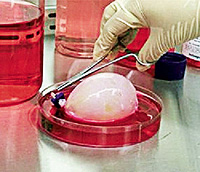
«Путем биопсии можно взять кусочек ткани, а спустя два месяца ее количество умножится в несколько раз, — объясняет директор института регенеративной медицины Энтони Атала. — Исходный материал и особые вещества мы кладем в специальную форму, оставляем в специальном лабораторном инкубаторе и через несколько недель получаем готовый орган, который уже можно пересаживать». Первую трансплантацию провели еще в конце 90-х. Операцию по пересадке мочевого пузыря сделали семи пациентам. Результаты оправдали ожидания ученых, и сейчас специалисты разрабатывают методы создания еще 20-ти органов — среди них сердце, печень, кровеносные сосуды и поджелудочная железа.
В 2007 году стволовые клетки помогли британским ученым создать часть сердца человека

Весной 2007 года группе британских ученых, состоящая из физиков, биологов, инженеров, фармакологов, цитологов и опытных клиницистов, под руководством профессора кардиохирургии Магди Якуба впервые в истории удалось воссоздать одну из разновидностей тканей человеческого сердца при помощи стволовых клеток костного мозга. Эта ткань выполняет роль сердечных клапанов. Если дальнейшие испытания пройдут успешно, разработанную методику можно будет применять для выращивания из стволовых клеток полноценного сердца для трансплантации больным.
В 2007 году японские ученые вырастили из стволовых клеток роговицу глаза

Весной 2007 года на симпозиуме по вопросам репродуктивной медицины в городе Иокогама были обнародованы результаты уникального эксперимента специалистов Токийского университета. Исследователи использовали стволовую клетку, взятую из края роговицы. Такие клетки способны развиваться в различные ткани, выполняя в организме восстановительные функции. Выделенная клетка была помещена в питательную среду. Спустя неделю она развилась в группу клеток, а на четвертой неделе преобразовалась в роговицу диаметром 2 см. Таким же образом был получен тонкий защитный слой (конъюнктива), покрывающий роговицу снаружи.
Ученые подчеркивают, что впервые полноценная ткань человеческого организма выращена из единственной клетки. Пересадка органов, полученных новым способом, исключает риск переноса инфекций. Японские ученые намерены приступить к клиническим испытаниям сразу после того, как удостоверяться в безопасности новой технологии.
В 2007 году японские ученые вырастили зуб из стволовых клеток
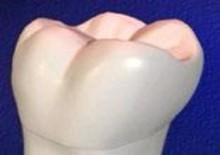
Японским ученым удалось вырастить зуб из одной клетки. Его вырастили в лабораторных условиях и пересадили мыши. Инъекция клеточного материала была произведена в коллагеновый каркас. После выращивания оказалось, что зуб принял зрелую форму, которая состояла из полноценных частей, таких как дентин, пульпа, сосуды, периодонтальные ткани, и эмаль. По словам исследователей, зуб был идентичен естественному. После трансплантации зуба лабораторной мыши он прижился и функционировал полностью нормально. Данный метод позволит выращивать целые органы из одной-двух клеток, говорят исследователи.
В 2008 году американские ученые смогли вырастить новое сердце на каркасе от старого

Дорис Тейлор (Doris Taylor) и её коллеги из университета Миннесоты (University of Minnesota) создали живое сердце крысы, используя необычную технику. Ученые взяли взрослое сердце крысы и поместили его в специальный раствор, который удалил из сердца все клетки мышечной сердечной ткани, оставив другие ткани нетронутыми. Этот очищенный каркас был засеян клетками сердечной мышцы, взятыми у новорождённой крысы, и помещён в среду, имитирующую условия в организме.
Всего через четыре дня клетки размножились настолько, что начались сокращения новой ткани, а через восемь дней реконструированное сердце уже могло качать кровь, хотя и всего на 2-процентном уровне мощности (считая от здорового взрослого сердца). Таким образом, учёные получили работоспособный орган из клеток второго животного. Этим путём в будущем можно было бы обрабатывать сердца, взятые для пересадки, для исключения отторжения органа. «Так вы можете сделать любой орган: почку, печень, лёгкое, поджелудочную железу», — говорит Тейлор. Донорский каркас, определяющий форму и структуру органа, будет наполняться родными для больного специализированными клетками, сделанными из стволовых.
Любопытно, что в случае с сердцем в качестве основы можно попробовать взять сердце свиньи, анатомически близкое к человеческому. Удалив только мышечную ткань, прочие ткани такого органа можно будет уже дополнить культивированными человеческими клетками сердечной мышцы, получив гибридный орган, который, по идее, должен хорошо прижиться. А новые клетки будут сразу хорошо снабжаться кислородом — благодаря старым сосудам и капиллярам, оставшимся от сердца донора.
Искусственные органы: человек умеет все


Основания для оптимизма, конечно же, есть. В наши дни в науке наметилось несколько направлений, которые, возможно, позволят в близком или дальнем будущем превратить Homo sapiens в более долговечную и надежную мыслящую конструкцию. Первое — это создание электронно-механических «подпорок» для недужного тела. Речь идет о роботизированных бионических протезах конечностей, достоверно воспроизводящих человеческую локомоторику, или даже целых экзоскелетах, которые смогут подарить радость движения парализованным.
 Мозг Выращивание нервной ткани — наиболее сложно из-за многообразия типов составляющих ее клеток и их сложной пространственной организации. Однако на сегодня существует успешный опыт выращивания аденогипофиза мыши из скопления стволовых клеток.
Мозг Выращивание нервной ткани — наиболее сложно из-за многообразия типов составляющих ее клеток и их сложной пространственной организации. Однако на сегодня существует успешный опыт выращивания аденогипофиза мыши из скопления стволовых клеток.
Эти хитроумные изделия дополнит нейромашинный интерфейс, который позволит считывать команды прямо с соответствующих участков головного мозга. Действующие прототипы подобных устройств уже созданы, теперь главное — их совершенствование и постепенное удешевление.
Вторым направлением можно считать исследования генетических и прочих микробиологических процессов, вызывающих старение. Познание этих процессов, возможно, в будущем даст возможность затормозить увядание организма и продлить активную жизнь за вековой предел, а возможно, и далее.
 Глаз Поиски ведутся в нескольких направлениях. Одно из них — бионический глаз: электронная камера плюс чип, имплантированный в сетчатку. Есть и некоторые успехи в выращивании сетчатки (пока у мышей).
Глаз Поиски ведутся в нескольких направлениях. Одно из них — бионический глаз: электронная камера плюс чип, имплантированный в сетчатку. Есть и некоторые успехи в выращивании сетчатки (пока у мышей).
И наконец, к третьему направлению относятся исследования в области создания подлинных запчастей к человеческому телу — тканей и органов, которые структурно и функционально будут мало чем отличаться от природных и позволят своевременно «отремонтировать» организм, пораженный тяжелой болезнью или возрастными изменениями. Известия о новых шагах в этой области приходят сегодня едва ли не ежедневно.

Запускаем печать
Базовая технология выращивания органов, или тканевой инженерии, заключается в использовании эмбриональных стволовых клеток для получения специализированных клеток той или иной ткани, например гепатоцитов — клеток паренхимы (внутренней среды) печени. Эти клетки затем помещаются внутрь структуры соединительной межклеточной ткани, состоящей преимущественно из белка коллагена.
 Сердце Наряду с созданием электронно-механических протезов ведется поиск более естественного имплантата, объединяющего в себе выращенные ткани сердечной мускулатуры с наноэлектронной системой контроля.
Сердце Наряду с созданием электронно-механических протезов ведется поиск более естественного имплантата, объединяющего в себе выращенные ткани сердечной мускулатуры с наноэлектронной системой контроля.
Таким образом обеспечивается заполнение клетками всего объема выращиваемого органа. Матрицу из коллагена можно получить путем очистки от клеток донорской биологической ткани или, что гораздо проще и удобнее, создать ее искусственным путем из биоразрушаемых полимеров или специальной керамики, если речь идет о кости. В матрицу помимо клеток вводятся питательные вещества и факторы роста, после чего клетки формируют единый орган или некую «заплатку», призванную заместить собой пораженную часть.
Правда, выращивание искусственной печени, легкого и других жизненно важных органов для пересадки человеку сегодня пока недостижимо, в более простых случаях такая методика успешно применяется. Известен случай пересадки пациентке выращенной трахеи, осуществленной в РНЦ хирургии им. Б.В. Петровского под руководством итальянского профессора П. Маккиарини. В данном случае в качестве основы была взята донорская трахея, которую тщательно очистили от клеток. На их место были введены стволовые клетки, взятые из костного мозга самой пациентки. Туда же были помещены факторы роста и фрагменты слизистой оболочки — их также позаимствовали из поврежденной трахеи женщины, которую предстояло спасти.
 Легкие Проведены успешные эксперименты по имплантации крысе легкого, выращенного на очищенной от клеток донорской матрице.
Легкие Проведены успешные эксперименты по имплантации крысе легкого, выращенного на очищенной от клеток донорской матрице.
Недифференцированные клетки в таких условиях дали начало клетками дыхательного эпителия. Выращенный орган имплантировали пациентке, причем были приняты специальные меры для проращивания имплантата кровеносными сосудами и восстановления кровообращения.
Впрочем, уже существует метод выращивания тканей без применения матриц искусственного или биологического происхождения. Метод нашел воплощение в устройстве, известном как биопринтер. В наши дни биопринтеры «выходят из возраста» опытных образцов, и появляются мелкосерийные модели. Например, аппарат компании Organovo способен распечатать фрагменты тканей, содержащих 20 и более клеточных слоев (причем туда входят клетки разных типов), объединенных межклеточной тканью и сетью кровеносных капилляров.
 Печень До выращивания целой искусственной печени еще далеко, однако фрагменты ткани печени человека уже получены методом выращивания на матрице из биоразлагаемых полимеров. Такие имплантаты смогут помочь в восстановлении пораженных участков.
Печень До выращивания целой искусственной печени еще далеко, однако фрагменты ткани печени человека уже получены методом выращивания на матрице из биоразлагаемых полимеров. Такие имплантаты смогут помочь в восстановлении пораженных участков.
Соединительная ткань и клетки собираются воедино по той же технологии, которую используют при трехмерной печати: движущаяся головка, позиционирующаяся с микронной точностью в трехмерной сети координат, «выплевывает» в нужную точку капельки, содержащие либо клетки, либо коллаген и другие вещества. Разные производители биопринтеров сообщили, что их устройства уже способны распечатывать фрагменты кожи подопытных животных, а также элементы почечной ткани. Причем в результате удалось достичь правильного расположения клеток разных типов друг относительно друга. Правда, эпохи, когда принтеры в клиниках будут способны создавать органы разного назначения и больших объемов, придется еще подождать.

Мозг под замену
Развитие темы запчастей для человека неизбежно приводит нас к теме самого сокровенного — того, что делает человека человеком. Замена мозга — пожалуй, самая фантастическая идея, касающаяся потенциального бессмертия. Проблема, как нетрудно догадаться, в том, что мозг — похоже, самый сложный из известных человечеству материальных объектов во Вселенной. И, возможно, один из самых непонятных. Известно, из чего он состоит, но очень мало известно о том, как он работает.
 Новая кожа Новая кожа. Сотрудник лаборатории достает из ванночки полоску искусственно выращенного эпидермиса. Ткань создали в дерматологическом институте в г. Помеция, Италия, под руководством профессора Микеле де Лука.
Новая кожа Новая кожа. Сотрудник лаборатории достает из ванночки полоску искусственно выращенного эпидермиса. Ткань создали в дерматологическом институте в г. Помеция, Италия, под руководством профессора Микеле де Лука.
Таким образом, если мозг удастся воссоздать как совокупность нейронов, устанавливающих друг с другом связи, надо еще придумать, как поместить в него всю необходимую человеку информацию. Иначе в лучшем случае мы получим взрослого человека с «серым веществом» младенца. Несмотря на всю сверхфантастичность конечной цели, наука активно работает над проблемой регенерации нервной ткани. В конце концов, цель может быть и скромнее — например, восстановление части мозга, разрушенной в результате травмы или тяжелого заболевания.
Проблема искусственной регенерации мозговой ткани усугубляется тем, что мозг обладает высокой гетерогенностью: в нем присутствует множество типов нервных клеток, в частности тормозные и возбуждающие нейроны и нейроглия (буквально — «нервный клей») — совокупность вспомогательных клеток нервной системы. Кроме того, разные типы клеток определенным образом расположены в трехмерном пространстве, и это расположение необходимо воспроизвести.
 Трахея Это тот самый случай, когда технологии выращивания тканей уже работают в медицине и спасают жизни людей. Известны случаи успешной имплантации трахеи, выращенной на донорской матрице из клеток спинного мозга пациента.
Трахея Это тот самый случай, когда технологии выращивания тканей уже работают в медицине и спасают жизни людей. Известны случаи успешной имплантации трахеи, выращенной на донорской матрице из клеток спинного мозга пациента.
Нервный чип
В одной из лабораторий знаменитого Массачусетского технологического института, известного своими разработками в сфере информационных технологий, подошли к созданию искусственной нервной ткани «по-компьютерному», применив элементы технологии изготовления микрочипов.
Исследователи из Бостона взяли смесь нервных клеток, полученных из первичной коры мозга крысы, и нанесли их на тончайшие пластины гидрогеля. Пластины образовали своего рода сэндвич, и теперь задача состояла в том, чтобы вычленить из него отдельные блоки с заданной пространственной структурой. Получив такие прозрачные блоки, ученые намеревались изучать процессы возникновения нервных связей внутри каждого из них.
 Мочевой пузырь Технология пересадки человеку мочевого пузыря, выращенного на коллагеновой матрицы из мочевого пузыря или тонкой кишки животного происхождения, уже создана и имеет положительную практику применения.
Мочевой пузырь Технология пересадки человеку мочевого пузыря, выращенного на коллагеновой матрицы из мочевого пузыря или тонкой кишки животного происхождения, уже создана и имеет положительную практику применения.
Задача была решена с помощью фотолитографии. На пласты гидрогеля накладывались пластиковые маски, которые позволяли свету воздействовать лишь на определенные участки, «сваривая» их воедино. Так удалось получить разнообразные по размерам и толщине композиции клеточного материала. Изучение этих «кирпичиков» со временем может привести к созданию значимых фрагментов нервной ткани для использования в имплантах.
Если инженеры MIT подходят к изучению и воссозданию нервной ткани в инженерном стиле, то есть механически формируя нужные структуры, то в Центре биологии развития RIKEN в японском городе Кобе ученые под руководством профессора Йошики Сасаи нащупывают другой путь — evo-devo, путь эволюции развития. Если плюрипотентные стволовые клетки эмбриона могут при делении создавать самоорганизующиеся структуры специализированных клеток (то есть разнообразные органы и ткани), то нельзя ли, постигнув законы такого развития, направлять работу стволовых клеток для создания имплантатов уже с природными формами?
 Позвоночник В деле выращивания костей и хрящей на матрицах достигнут большой прогресс, однако восстановление нервной ткани спинного мозга — дело будущего.
Позвоночник В деле выращивания костей и хрящей на матрицах достигнут большой прогресс, однако восстановление нервной ткани спинного мозга — дело будущего.
И вот главный вопрос, на который намеревались найти ответ японские биологи: насколько зависит развитие конкретных клеток от внешних факторов (например, от контакта с соседними тканями), а в какой степени программа «зашита» внутри самих стволовых клеток. Исследования показали, что есть возможность вырастить из изолированной группы стволовых клеток заданный специализированный элемент организма, хотя внешние факторы играют определенную роль — например, необходимы определенные химические индуцирующие сигналы, заставляющие стволовые клетки развиваться, скажем, именно как нервная ткань. И для этого не понадобится никаких поддерживающих структур, которые придется наполнять клетками — формы возникнут сами в процессе развития, в ходе деления клеток.
В новом теле

Вопрос о пересадке мозга, коль скоро мозг является вместилищем интеллекта и самого человеческого «я», по сути, не имеет смысла, так как если мозг уничтожен, то воссоздать личность невозможно (если только со временем не научатся делать «резервные копии» сознания). Единственное, что могло бы иметь резон — это пересадка головы, а точнее — пересадка тела голове, у которой с телом проблемы. Однако при невозможности на современном уровне медицины восстановления спинного мозга, тело с новой головой останется парализованным. Правда, по мере развития тканевой инженерии, возможно, нервную ткань спинного мозга можно будет восстанавливать с помощью стволовых клеток. На время операции мозг придется резко охлаждать для предотвращения смерти нейронов.
По запатентованной Сасаи методике японцам удалось вырастить трехмерные структуры нервной ткани, первой из которых стала полученная из эмбриональных стволовых клеток мышей сетчатка глаза (так называемый зрительный бокал), которая состояла из функционально различных типов клеток. Они были расположены так, как предписывает природа. Следующим достижением стал аденогипофиз, не просто повторяющий структуру природного, но и выделяющий при пересадке мыши необходимые гормоны.

Разумеется, до полнофункциональных имплантов нервной ткани, а тем более участков человеческого мозга еще очень и очень далеко. Однако успехи искусственной регенерации тканей с применением технологий эволюции развития указывают путь, по которому пойдет вся регенеративная медицина: от «умных» протезов — к композитным имплантатам, в которых готовые пространственные структуры «проращиваются» клеточным материалом, и далее — к выращиванию запасных частей для человека по тем же законам, по которым они развиваются в естественных условиях.
Выращивание тканей и органов: мифы и реальность (лекция)


В Москве при поддержке Фонда «Росконгресс» и телеканала «Доктор» 4-5 октября прошел X форум VESTIFINANCE, который продолжил серию выступлений известных российских экспертов на тему «Следующие 20 лет». Юбилейный форум был посвящен одной из самых значимых для каждого человека тем – здоровью и развитию медицины будущего. Новые средства лечения рака, будущее фармацевтики, клонирование человека и редактирование ДНК, выращивание органов и тканей — эти и другие вопросы были подняты на форуме. Второй день форума открыло выступление Петра Тимашева, директора Института регенеративной медицины Сеченовского университета. Спикер рассказал все о выращивании тканей и органов.
Проблема нехватки донорских органов для пересадки заставляет искать биомедицинские решения, не требующие использования донорского материала. Технологии регенеративной медицины на сегодняшний день считаются наиболее перспективными. К ним относят генную и клеточную терапию и инжиниринг тканей.

Время ожидания донорских органов
Бурное развитие получило еще одно направление регенеративной медицины — биопринтинг, когда ткани и органы создают из конгломератов клеток, подобно конструктору. Биопечать происходит с использованием специально разработанных 3D-биопринтеров, подобно тому, как печатают на 3D-принтерах различные детали — послойно, по цифровой трехмерной модели.
Картриджи принтеров при этом заправляют сфероидами — конгломератами клеток, которые наносят на специальную подложку — своеобразную биобумагу. Напечатав один слой из клеточных сфероидов, сверху наносят второй, который срастается с первым. Так постепенно получают объемный живой объект — ткань или орган.

Медицина всегда являлась драйвером развития технологий. С древнейших времен люди все время пытались придумать что-то, чтобы восстановить качество жизни. В Древнем Риме на место выпавшего зуба вставляли протез — такое открытие сделали археологи. Вот и сейчас, когда у нас выпадает зуб, мы идем к стоматологу и получаем примерно такой же протез; только сделан он из титана или керамики, но идея осталась древнеримской — взять и заменить какую-то часть человеческого тела искусственной. При этом протезы — зубные, суставные или искусственные сердечные клапаны — со временем требуют замены, а значит, повторной сложной операции.

Идея всей регенеративной медицины — попробовать отойти от использования традиционного подхода, когда мы вместо поврежденной ткани вставляем искусственную, которая со временем изнашивается. Эта область родилась на стыке нескольких направлений — биологии, медицины, физики, химии, инженерии, математики. Задача — запустить процесс восстановления ткани изнутри, поэтому парадигму регенеративной медицины обозначают как healing from inside – «излечение изнутри». Это определение наиболее емко показывает всю идею этого направления.

В биопринтинге есть два больших направления. Первое — это экструзионная печать. Первый принтер, который позволял печатать клеточными сфероидами, был разработан и создан в нашей российской фирме 3D Bioprinting Solutions. Существует также лазерный биопринтер, где лазерный луч индуцирует перенос клеток с донорной на акцепторную пластинку.

Пока рано говорить о том, что биопринтеры будут использоваться в клиниках. Пока речь идет о концепции биофабрики, когда от компьютерной модели, с использованием всех достижений (клеточных материалов для активных соединений, биореакторов) мы на выходе получаем ткань, которую можно в дальнейшем пересаживать.
Так, команда из Института регенеративной медицины Уэйк-Форест разработала методику, которая позволяет печатать ткань, пронизанную микроканалами, подобно губке, благодаря чему в ткани нормально проникают питательные вещества. Печать была осуществлена с помощью интегрированной печатной системы тканей и органов (Integrated Tissue-Organ Printing System, ITOP. Орган создается на основе из биоразлагаемого пластика. Сверху наносится гель на водной основе, который содержит клетки и стимулирует их рост.
После того как структуры имплантируются в животных, пластик постепенно замещается естественной структурной матрицей из белков, продуцируемых клетками. Также в имплантаты постепенно внедряются кровеносные сосуды и нервная ткань.
Результаты, по мнению ученых, оказались многообещающими. Ушные раковины, подсаженные мышам, спустя два месяца сохранили форму, а также в них на 20% увеличилось содержание гликозоаминогликанов, которые входят в состав клеточного матрикса. Мышечная ткань, вытянутая вдоль опорной конструкции, спустя две недели также сохранила свои механические характеристики.

Еще одно направление — бескаркасные подходы с использованием трехмерных клеточных систем. Это технологии тканевых сфероидов и клеточных пластов, когда без использования материалов мы создаем трехмерную структуру с использованием различных подходов. Главная идея в том, что никаких дополнительных искусственных материалов в эту структуру не вносится.
Суть метода биопечати в том, что будущий орган формируется из двух основных компонентов: живых клеток и клеточной матрицы, моделирующей условия межклеточной среды и соединительной ткани.
Выбор клеток для 3D-биопечати тканей или органов — важнейшее условие их правильного функционирования в созданном материале. В организме ткани и органы состоят из многочисленных типов клеток с особыми и необходимыми биологическими свойствами, что должны быть воспроизведены и в трансплантируемой ткани.

Откуда можно взять клетки? Костный мозг, жировая ткань, пульпа зуба, пуповинная кровь — все эти источники сейчас активно исследуется и сравниваются, какие лучше клетки подойдут для каких подходов. Источников клеток в нашем организме очень много, и правильное их использование может привести к тому, что мы сможем воссоздать любую ткань, которую захотим.

В настоящее время есть множество методов для формирования трехмерных структур. Возможно создать любой объект, с любой структурой, из любого материала. Дальше уже дело в деталях — скорость разрушения материала, механические свойства и т. д. Источники клеток могут быть превращены в различные типы клеток и тканей под воздействием биологически активных веществ. Прежде всего используются факторы роста, которые ускоряют, например, образование сосудов, также используются и наночастицы, гормоны, витамины, низкомолекулярные соединения.
При том количестве клеток, которое мы можем использовать для регенеративной медицины, при том количестве методов, биологически активных веществ необходимо провести множество исследований. С 2000 г. множество научных групп пытается сделать такую разработку, которая сначала бы хорошо себя показала в пробирке, потом на животном и потом в итоге нашла клиническое применение.

Вокруг регенеративной медицины сформировался миф, что клеточные технологии еще не скоро придут в клиническую практику. Это не так – достаточно посмотреть на количество зарегистрированных клинических исследований.

Сейчас Китай становится глобальным лидером не только по проведению и испытаниям на животных, но и по внедрению в клиниках. В Поднебесной счет сотни пациентов лечат с использованием клеточных технологий.

Существует также миф, что все стволовые клетки могут вызвать рак. Это не так. Только недифференцированные эмбриональные или индуцированные плюрипотентные стволовые клетки могут являться реальной прямой причиной развития опухоли и рака. Для остальных видов нет научных статей, подтверждающих этот миф. Часто используемые в клеточных технологиях мезенхимные стромальные клетки сами не дают начало опухолевым или раковым клеткам, но они имеют способность к миграции в опухоль, если она уже сформирована в организме. Продолжаются эксперименты с использованием клеток как носителей для доставки какого-то вещества в раковую опухоль. Если вводить клетки системно, то они будут концентрироваться в раковой опухоли и это может стать направленной доставкой какого-то лекарства в эту опухоль.

Разработка и внедрение в клиническую практику новых биотехнологических аналогов тканей и органов, в частности эквивалентов кожи человека, призванных временно или постоянно заменять поврежденные или разрушенные ткани, остается актуальной задачей регенеративной медицины. На данный момент существует несколько коммерческих продуктов, которые позволяют восстанавливать кожу. Вся процедура производства готового продукта стоит порядка $20-25 тыс. В течение двух-трех недель клетки пациента культивируются, далее их сажают на мембрану, и врачу доставляют уже готовую структуру, которую дальше он может применять для восстановления вашей кожи. Есть еще другой продукт – Apligraf, у которого применение чуть шире. Изделие состоит из живых клеток и структурных белков. Основной – дермальный слой – представлен фибробластами и коллагеном 1-го типа, верхний слой – кератиноцитами.

В 2006 г. группа профессора Энтони Атала опубликовала статью о восстановлении мочевого пузыря. Атала еще в 1999 г. пересадил нескольким пациентам мочевой пузырь, выращенный с использованием стволовых клеток, но не опубликовал тогда результаты, дабы убедиться, что операция прошла успешно в отдаленном периоде времени. С тех пор в мире проведено около 30 подобных операций.

Сейчас Атала – один из мировых лидеров нового направления в медицине, которое получило название тканевой инженерии. В его лабораториях ведутся работы над искусственным получением множества тканей и органов, не только урологических (несмотря на то что Атала – автор большой работы Stem Cell in Urology, опубликованной в 2008 г.). Здесь выращивают хрящи, кости, сосуды, уретру и многие другие органы, ткани.
Пытаются здесь работать и над почками, которые вырастить гораздо сложнее, чем мочевой пузырь. Сам профессор Атала возлагает большие надежды на технологию 3D-печати, посредством которой орган можно будет просто напечатать из соответствующих клеточных культур. Впрочем, более простые случаи клеточной недостаточности пытаются лечить, делая инъекции стволовых клеток в начинающую давать сбои почку.
Васкуляризацию (формирование новых кровеносных сосудов — обычно капилляров — внутри ткани) считают одной из главных проблем всей регенеративной медицины. Потому что, когда вы разрабатываете что-то маленькое, небольшое, то там проблема доставки питательных веществ не стоит, а когда идет масштабирование процесса, то доставка и кислорода, и активных субстанций уже проблема, потому что есть диффузионные ограничения.

Например, в одной из работ демонстрируется, как в черепе мышки с использованием искусственных материалов и клеток была восстановлена кость, а сосуд, который был проращен в этом материале, снабжал всеми питательными соединениями новообразованную кость.

Клетки, которые были внесены на этом искусственном, трехмерном конструкте в череп мышки, образовали сосуд. А вход в этот сосуд был образован клетками, которые принадлежали самой мышке. Возникает вопрос — почему именно в этом месте начал расти сосуд? Мы открыли совместно с университетом Питтсбурга направление регенеративной липидомики, где исследуются процессы взаимодействия между клетками «хозяина» и клетками «гостя» с использованием технологии липидов. Это фундаментальная наука, которая в дальнейшем нам позволит управляемо создавать в том числе сосуды и попробовать перейти ограничение по росту сосудов в материалах и в клетках, которые мы пересаживаем.

Если говорить о развитии регенеративной медицины в России, то стоит отметить давнюю проблему – в нашей стране до 2016 г. не было никаких законов, связанных с этой отраслью. Вторая была проблема — направление практически не поддерживалось государством, но сейчас выделяются деньги на эти исследования в рамках проекта национального проекта «Здоровье», в том числе и наши фонды — Российский фонд фундаментальных исследований, Российский научный фонд.

Еще одна проблема – языковой барьер. К сожалению, не очень хорошее знание английского порой мешает должны донести какие-то разработки до мирового сообщества. Важно, чтобы о тех исследованиях, которые мы делаем, знали люди не только в нашей лаборатории или в нашем университете, но и во всем мире.

Согласно базам Scopus и Clinicaltrials за десять лет количество публикаций в области регенеративной медицины увеличилось более чем 6-7 раз, и это здорово. Публикационная активность наблюдается в Томске, Новосибирске, Москве, Питере. Потом мы сравнили это с базами данных клинических исследований и поняли, что где-то исследования так и остаются только публикациями. Однако стало известно, что в Екатеринбурге и Челябинске проводят интересные исследования и публикуют в международной базе данных.


В 2016 г. в России был принят закон биомедицинских клеточных продуктах, который был призван обеспечить российских ученых и производителей регулированием, конкурентоспособным на международной арене и помогающим привлекать инвестиции в биотехнологические компании, зарегистрированные в России.

Закон ввел очень строгие ограничения, поэтому результатом пока явилось временное снижение количества новых клинических исследований в регенеративной медицине. Но я надеюсь, что это, конечно, временно. Согласно закону все биомедицинские клеточные продукты должны быть производиться в стандартах GCP (англ. good clinical practice — надлежащая клиническая практика) и GMP (англ. good manufacturing practic — надлежащая производственная практика).
Это сложное требование, и к настоящему времени всего одна компания зарегистрировала площадку для производства биомедицинских клеточных продуктов. Это очень важно, что закон регулирует импорт и экспорт биоматериалов (ткани, биологические жидкости и т. д.). Во всем мире это известная практика – законодательно регулировать сдачу биоматериала для создания биомедицинских клеточных продуктов.
У нас очень много исследований применения клеток, и практически нет исследований по применению материалов и клеток. Это связано с тем, что группы исследователей на настоящий момент разрознены: у нас нет объединения материаловедов, биологов и т. д. Пока 11% посвящено тканеинженерным скаффолдам, есть надежда, что эта цифра будет только расти.

Владимир Александрович Миронов – научный руководитель лаборатории 3D Bioprinting Solutions, профессор Университета Вирджинии, кандидат медицинских наук. Тканевый инженер, автор первой публикации о печати органов, он заложил основы развития биопринтинга во всем мире. Он же впервые создал целый орган, щитовидную железу, на принтере, который был разработан в компании 3D Bioprinting Solutions.

Первая операция, которая была проведена в конце 2018 г. с использованием клеточных сфероидов и коллагеновой мембраны на пациенте у которого была стриктура уретры.

Вместо того, чтобы брать материал из щеки, были взяты его клетки, и с их использованием была выращена конструкция органа. К слову, возраст пациента – 69 лет. Этот пример развенчивает миф о том, что регенеративная медицина подходит только молодым.
В России обещают начать применять искусственные органы в трансплантологии
Искусственные человеческие органы скоро станут выращивать в строящейся при Военно-медицинской академии имени Кирова клинике в Санкт-Петербурге. Решение о строительстве клиники принял министр обороны. Многопрофильный центр планируют оснастить самым современным оборудованием, которое позволит самым подробным образом изучать стволовые клетки. Научно-технический отдел, который займётся клеточными технологиями, уже сформирован.
«Основным направлением работы отдела станет создание биологического банка и создание возможностей для выращивания искусственных органов, — говорит начальник отдела организации научной работы и подготовки научно-педагогических кадров академии Евгений Ивченко. — Российские учёные давно работают над искусственными органами».
Два года назад завотделом Федерального научного центра трансплантологии и искусственных органов имени академика В.И. Шумакова Мурат Шагидулин сообщил о создании искусственного аналога печени, пригодного для пересадки. Учёные смогли получить искусственную печень и протестировать её в доклинических условиях. Орган вырастили на основе бесклеточного каркаса печени, из которой заранее по специальной технологии удалили все ткани. Остались только белковые структуры кровеносных сосудов и других компонентов органа. Каркас засеяли аутологичными клетками костного мозга и печени. Эксперименты на животных показали: если выращенный элемент имплантировали в печень или брызжейку тонкой кишки, он способствовал регенерации тканей и давал полное восстановление функции повреждённого органа. Животные представляли собой модели острой и хронической печёночной недостаточности. И выращенный элемент позволял увеличить выживаемость в два раза. Спустя год после имплантации все животные были ещё живы. Между тем в контрольной группе умерло около 50% особей. Через семь дней после имплантации в основной группе биохимические показатели функции печени уже были на уровне нормы. По прошествии 90 дней после пересадки в брызжейку тонкой кишки учёные нашли там жизнеспособные гепатоциты и новые сосуды, которые проросли через каркас элемента.
«Исследования в области создания таких сложных биоинженерных органов, как печень, почки, лёгкие и сердце, в последние годы ведутся в ведущих научных лабораториях США и Японии, но дальше стадии изучения на животной модели они пока не продвинулись, — комментирует заведующий отделом экспериментальной трансплантологии и искусственных органов Центра Мурат Шагидулин. — Наши опыты на животных прошли хорошо. Спустя три месяца после трансплантации в телах животных обнаружили здоровые клетки печени и новые кровеносные сосуды. Это говорило о протекавшем процессе регенерации пересаженной печени и том, что она прижилась».
Японские учёные из Университета Йокогамы сумели вырастить печень размером в несколько миллиметров. Они смогли сделать это благодаря индуцированным плюрипотентным стволовым клеткам (iPSCs). Выращенная печень работает как полноценный орган. По словам руководителя исследовательской группы профессора Хидэки Танигути, минипечень справляется с переработкой вредных веществ столь же эффективно, что и реальный человеческий орган. Учёные надеются начать клинические испытания искусственной печени в 2019 г. Новые, созданные в лаборатории органы, будут пересаживать пациентам с тяжёлыми заболеваниями печени для поддержания её нормальных функций.
Несколько ранее японские учёные лабораторным путём почти приблизились к новейшему открытию — созданию полностью функционирующих почек, способных заменить настоящие. До этого прототипы искусственной почки создавались. Но им не удавалось нормально выводить мочу (раздувались от давления). Однако японцы исправили ситуацию. Специалисты уже вполне успешно пересаживают искусственные почки свиньям и крысам.
Доктор Такаси Йооко и его коллеги из Медицинской школы Университета Дзинкей использовали стволовые клетки, но не просто вырастили ткани почки, а вырастили и дренажную трубку, и мочевой пузырь. В свою очередь, крысы, а потом и свиньи, были инкубаторами, в которых уже развивалась и росла эмбриональная ткань. Когда новую почку соединили с существовавшим в теле животных мочевым пузырем, система заработала в целом. Моча шла из пересаженной почки в пересаженный мочевой пузырь, и лишь после этого она попадала в мочевой пузырь животного. Как показали наблюдения, система работала и через восемь недель после трансплантации.
По словам учёных, в перспективе, возможно, удастся создать и полноценные имплантаты голосовых связок для людей. Исследователи собрали фрагменты ткани четырёх людей, страдающих проблемами с голосовыми связками. Этим пациентам связки были удалены. Была также забрана ткань у одного умершего донора. Специалисты изолировали, очистили и вырастили клетки слизистой оболочки в особой трёхмерной структуре, имитирующей среду тела человека. Примерно за две недели клетки срослись и сформировали ткань, напоминающую по эластичности и клейкости реальные голосовые связки. Потом специалисты присоединили полученные голосовые связки к искусственной трахее и пропустили через них увлажнённый воздух. Когда воздух доходил до связок, ткани вибрировали и продуцировали звук, как бы это происходило при нормальных условиях в организме. В ближайшее время врачи ждут закрепления полученного результата на нуждающихся в нём людях.
Стволовые клетки и выращивание тканей и органов
Прежде, чем приступить к обсуждению темы статьи, хочу сделать небольшой экскурс, что представляет собой организм человека. Это поможет понять, как важна работа любого звена в сложной системе человеческого организма, что может произойти при сбое, и как современная медицина пытается решить проблемы, если какой-либо орган выходит из строя.
Организм человека как биологическая система
Человеческий организм – это сложная биологическая система, имеющая особую структуру и наделенная специфическими функциями. Внутри этой системы различают несколько уровней организации. Высшая интеграция – это организменный уровень. Далее по нисходящей идут системный, органный, тканевой, клеточный и молекулярный уровни организации. От согласованной работы всех уровней системы зависит слаженная работа всего организма человека.
Если какой-то орган или система органов работает неправильно, то нарушения касаются и более низших уровней организации, таких как ткани и клетки.
Молекулярный уровень – это первый кирпичик. Как следует из названия, весь организм человека, как и всего живого, состоит из бесчисленного множества молекул.
Клеточный уровень можно себе представить как разнообразный компонентный состав молекул, образующих разные клетки.
Клетки, объединенные в разные по морфологии и функционированию ткани, образуют тканевой уровень.
В состав органов человека входят разнообразные ткани. Они обеспечивают нормальное функционирование какого-либо органа. Это – органный уровень организации.
Следующий уровень организации – системный. Определенные анатомически объединенные органы выполняют более сложную функцию. Например, пищеварительная система, состоящая из различных органов, обеспечивает переваривание поступающей в организм пищи, всасывание продуктов пищеварения и выведение неиспользованных остатков.
И высший уровень организации – организменный уровень. Все системы и подсистемы организма работают, как хорошо настроенный музыкальный инструмент. Согласованная работа всех уровней достигается благодаря механизму саморегуляции, т.е. поддержки на определенном уровне различных биологических показателей. При малейшем дисбалансе в работе какого-либо уровня организм человека начинает работать с перебоями.
Что такое стволовые клетки?
Термин «стволовые клетки» был введен в науку русским гистологом А. Максимовым в 1908 году. Стволовые клетки (СК) – это неспециализированные клетки. Их еще рассматривают как незрелые клетки. Они имеются практически у всех многоклеточных, включая человека. Путем деления клетки себя воспроизводят. Они способны превращаться в специализированные клетки, т.е. из них могут образовываться различные ткани и органы.
Самое большое количество СК у младенцев и детей, в юности количество стволовых клеток в организме уменьшается в 10 раз, а зрелому возрасту – в 50 раз! Значительное уменьшение числа СК в ходе старения, а также тяжелых заболеваний уменьшает возможности организма к самовосстановлению. Отсюда следует неприятный вывод: жизнедеятельность многих важных систем органов снижается.
Стволовые клетки и будущее медицины
Ученые- медики давно обратили внимание на пластичность СК и теоретическую возможность выращивать из них различные ткани и органы человеческого организма. Работы по изучению свойств СК начались во второй половине прошлого века. Как всегда, первые исследования проводились на лабораторных животных. К началу нашего века начались попытки, использовать СК для выращивания тканей и органов человека. Хочу рассказать о наиболее интересных результатах в этом направлении.
Японским ученым в 2004 г. удалось вырастить в лабораторных условиях капиллярные кровеносные сосуды из СК.
В следующем году американским исследователям из университета штата Флорида удалось вырастить из СК клетки головного мозга. Ученые заявили, что такие клетки способны вживляться в головной мозг, и их можно использовать при лечении таких заболеваний, как болезни Паркинсона и Альцгеймера.
В 2006 швейцарские ученые из университета Цюриха вырастили в своей лаборатории клапаны сердца человека. Для этого эксперимента использовались СК из околоплодной жидкости. Доктор С. Хёрстрап полагает, что эта методика может быть использована для выращивания сердечных клапанов для еще не родившегося ребенка, у которого обнаружены дефекты сердца. После рождения младенцу можно пересадить новые клапаны, выращенные из стволовых клеток околоплодной жидкости.
В том же году американские медики вырастили в лабораторных условиях целый орган – мочевой пузырь. СК были взяты у человека, для которого выращивался этот орган. Доктор Э. Атала, директор института регенеративной медицины, рассказал, что клетки и специальные вещества помещаются в особую форму, которая остается в инкубаторе в течение нескольких недель. После этого готовый орган пересаживается пациенту. Такие операции делаются сейчас в обычном режиме.
В 2007 на международном медицинском симпозиуме в Иокагаме были представлен доклад японских специалистов из университета Токио об удивительном научном эксперименте. Из единственной стволовой клетки, взятой из роговицы и помещенной в питательную среду, удалось вырастить новую роговицу. Ученые намеревались приступить к клиническим исследованиям и в дальнейшем применять эту технологию при лечении глаз.
Японцам принадлежит пальма первенства в выращивании зуба из единственной клетки. СК пересадили на коллагеновый каркас и начали эксперимент. После выращивания зуб выглядел как естественный и имел все составляющие, включая дентин, сосуды, эмаль и т.д. Зуб был трансплантирован лабораторной мыши, прижился и функционировал нормально. Японские ученые видят большие перспективы применения этого метода в выращивании зуба из одной СК с последующей пересадкой его хозяину клетки.
Японским медикам из университета Киото удалось получить из СК ткани почек, надпочечников и фрагмент почечного канальца.
Ежегодно во всем мире миллионы людей умирают от заболеваний сердца, головного мозга, почек, печени, мышечной дистрофии и т.д. В их лечении могут помочь стволовые клетки. Однако, существует один момент, который может затормозить применение стволовых клеток в медицинской практике – это отсутствие международной законодательной базы: откуда можно брать материал, сколько его можно хранить, как должны взаимодействовать пациент и его доктор при использовании СК.
Вероятно, проведение медицинских экспериментов и разработка такого закона должны идти параллельно.
Как вам статья?